Оглавление
Жесткость воды что это такое — практические советы по нормализации

Жесткость – это свойство воды, которое определяет ее потребительские качества и имеет важное хозяйственное значение. В процессе кипячения жесткая жидкость образует накипь на стенках и внутренних деталях нагревательных приборов, что вызывает ухудшение теплотехнических характеристик бытовой техники
В процессе кипячения жесткая жидкость образует накипь на стенках и внутренних деталях нагревательных приборов, что вызывает ухудшение теплотехнических характеристик бытовой техники.
Не особенно подходит она и для стирки, поскольку способствует снижению очищающих характеристик моющих средств и увеличивает их расход.
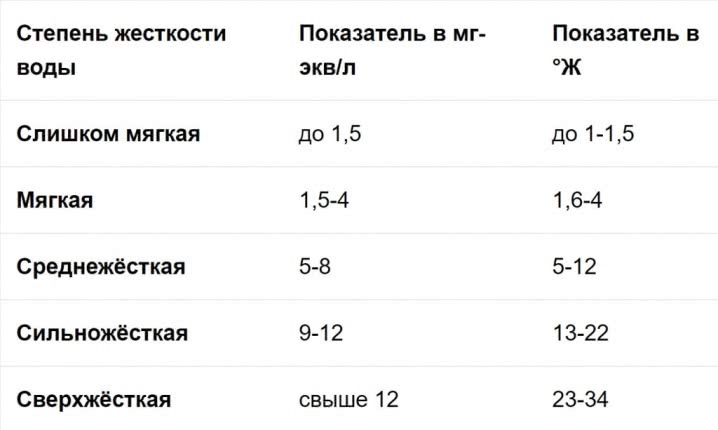
| Градусы dH | Характер воды | Жесткость в мг. х экв/л. | Эквивалент в mg/L |
| 23 — 34° | Очень жесткая | выше 12 мг х экв/л | 320 — 530 ppm |
| 13 — 22° | Жесткая | 8 – 12 мг х экв/л | 210 — 320 ppm |
| 9 — 12° | Средней жесткости | 4 – 8 мг х экв/л | 140 — 210 ppm |
| 5 — 8° | Мягкая | 1,5 – 4 мг х экв/л | 70 — 140 ppm |
| 0 — 4° | Очень мягкая | До 1,5 мг х экв/л | 0 — 70 ppm |
Откуда берется высокая жесткость? Ее определяет наличие солей магния и кальция – химических компонентов, выполняющих роль активных регуляторов различных химических процессов в окружающей среде. Естественно, что жидкость, которая берется из разных водоемов, может иметь ту или иную степень жесткости.
При этом река, озеро и любой другой источник пополняются из подземных источников, протекающих в известняковых пластах. Проходя через них, вода обогащается солями жесткости, а значит, будет жесткой. Для сравнения – данный показатель у поверхностных вод всегда заметно ниже, чем у подземных. Жесткость воды в природных источниках постоянно изменяется.
Максимальных отметок она достигает зимой, а минимальных – весной, во время таяния снегов.
Таким образом, жесткой является та вода, которая содержит соли магния и кальция в больших количествах. Кстати, магниевые соли растворяются хуже кальциевых, и жидкость с их высоким содержанием имеет выраженный горький вкус.
Шкала жесткости воды
Выделяются следующие виды жесткости:
- Общая – определяется как суммарная концентрация ионов магния и кальция.
- Карбонатная – зависит от наличия в воде карбонатов, гидрокарбонатов кальция и магния. Практически полностью устраняется в ходе кипячения, поэтому второе название карбонатной жесткости – временная. В процессе нагрева гидрокарбонаты распадаются – образуется угольная кислота, а карбонаты кальция, гидроксиды магния выпадают в виде осадка.
- Некарбонатная – обусловлена присутствием магниевых и кальциевых кислотных солей. При кипячении не устраняется (то есть является постоянной).
Общая жесткость измеряется в GH.
GH показывает суммарное содержание щелочноземельных металлов в виде ионов. Для примера – в воде, значение GH которой близкое к нулю, аквариумные рыбки не живут, употреблять ее в пищевых целях также не рекомендуется.
В мире для измерения показателей жесткости используются разные значения. В России Госстандарт установил следующий показатель – моль на кубический метр.
Числовое значение жесткости, которое выражается в молях на кубический метр, равняется числовому значению жесткости в миллиграмм-эквивалентах на литр.
На западе используют немецкий (d°, dH), французский (f°), американский (ppm CaCO3) градусы.
Влияние жесткости воды, нормативные требования и рекомендации
Какую воду можно употреблять для приготовления пищи и питья? Требования относительно жесткости жидкости зависят от условий конкретной местности. Учтите, что слишком жесткая вода имеет горький вкус и негативно влияет на работу органов пищеварения.
ВОЗ конкретные цифры не называет, хотя исследований на тему связи качества воды с заболеваниями сердца, сосудов и других органов организма проводились неоднократно. Слишком мягкая вода – это тоже плохо, поскольку она нарушает водно-солевой баланс.
Жидкость с жесткостью от 4 мг-экв/ чревата – главная причина образования накипи на внутренних деталях отопительных систем. Вредна она и для кожи, волос.
Жесткость – важный параметр воды, который зависит от количества и типа растворенных в ней минеральных веществ. Смягчение следует делать только после предварительного анализа. Почему? Потому что не все методы смягчения снижают содержание минеральных веществ – они могут просто превращать соли жесткости в соли, которые никак не влияют на рассматриваемый показатель.
Классификация воды по жетскости
В России жесткость воды измеряют в градусах жесткости, но она так же может быть выражена в объемной доле или массовым числом.
Официально принятая единица измерения, которая используется в системе СИ (международная система единиц) – моль на кубический метр. Но на практике не используют перечисленные единицы измерения, предпочитая миллиэквивалент на литр (мг-экв./л).
По уровню жесткости воду делят на четыре типа:
- Мягкая вода (менее 2 миллиэквивалентов на литр);
- Нормальная вода (от 2 до 4 миллиэквивалентов на литр);
- Жесткая вода (от 4 до 6 миллиэквивалентов на литр);
- Очень жесткая вода (6 и более миллиэквивалентов на литр).
Эта классификация называется американской и при оценке жесткости воды используется чаще всего.
Подобная классификация есть и в градусах жесткости, но представляет она только 3 типа воды:
- Мягкая вода (менее 2 градусов жесткости);
- Вода средней жесткости (от 2 до 10 градусов жесткости);
- Крайне жесткая вода (от 10 градусов жесткости и больше).
Нормы жесткости воды
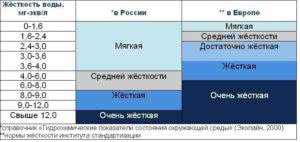
Нормы жесткости воды в России и мире сильно отличаются друг от друга. В России разрешена вода, жесткость которой не превышает порог в 7 миллиэквивалентов на литр, то есть, не запрещается подавать населению очень жесткую воду.
Те же показатели в Европе не могут быть больше 1,2 миллиэквивалентов на литр. Это значит, что европейцы пьют мягкую воду, жесткость которой почти в шесть раз меньше установленной в России.
Типы жесткости воды по восприимчивости к термообработке.
Первый тип – временная жесткость, когда помимо кальция и магния, в воде обнаруживаются гидрокарбонатные анионы. Ее так же называют карбонатной. Она легко удаляется при кипячении воды и никак не влияет на организм человека.
Второй тип – постоянная жесткость, еще называемая некарбонатной жесткостью. Она обусловлена наличием соединений кальция и магния, образованных в результате взаимодействия с сильными кислотами, например, серной или азотной. Такая жесткость не удаляется при кипячении воды, потому что не соли подобного типа не распадаются под воздействием температуры.
Общая жесткость воды вычисляется путем суммирования показателей карбонатной и некарбонатной жесткости.
Самые высокие показатели жесткости из-за обилия растворенных солей определяют в морской и океанической воде. Жесткость поверхностных вод обычно в несколько раз меньше грунтовых вод и влаги из подземных источников.
Как определить жесткость воды с помощью хозяйственного мыла?
Есть еще один увлекательный опыт, который можно провести дома, чтобы определить жесткость воды. Он дает погрешность до 1-2°Ж.
- Возьмите 72% хозяйственное мыло. Допустимо и в 60%. Отмеряем ровно 1 г – это примерно 1/3 ч. л.
- Наливаем в стакан с горлышком шириной в 6 см немного дистиллированной воды
Совет: Проверьте все же воду для данного эксперимента. Не всегда покупная жидкость соответствует требованиям. Хоть незначительные, но возможны отклонения от нормы. Но в таком случае – опыт даст большую погрешность.
(буквально 10-12 мл) – это примерно на 2 см от низа. Опыт не очень точный, поэтому погрешность допускается, и небольшое расхождение в миллиметрах не страшно. Но для своего же удобства приклейте от начала внутреннего дна стакана бумажную линейку снаружи.
- Подогреваем воду, чтобы мыло быстрее растворилось, и всыпаем измельченный кусочек мыла. Аккуратно, с минимальным образованием пены перемешиваем до полного растворения.
- Теперь доливаем еще дистиллированной воды до отметки 7,2 см от внутреннего дна! Если у вас 60% мыло, то до черты в 6 см. Снова перемешиваем и при необходимости снимаем пену.
- Берем литровую банку, набираем 0,5 л тестируемой воды. Теперь аккуратно вливаем мыльную воду и активно помешиваем ложкой. Стоит добавлять мыльный раствор до тех пор, пока не образуется устойчивая пена. Таковой ее можно считать, если после прекращения перемешивания она сразу же не падает.
- Далее надо вычесть использованные сантиметры мыльной воды и перевести их нужные единицы измерения по таблице.
| Градусы dH | Характер воды | Жесткость в мг-экв/л |
| 0–4° | Очень мягкая | до 1,5 мг-экв/л |
| 5–8° | Мягкая | 1,5–4 мг-экв/л |
| 9–12° | Средней жесткости | 4–8 мг-экв/л |
| 13–22° | Жесткая | 8–12 мг-экв/л |
| 23–34° | Очень жесткая | выше 12 мг-экв/л |

Сравнение результатов
Как понизить жесткость воды в домашних условиях
Существуют разные методы удаления отложений солей. В домашних условиях можно воспользоваться теми, которые не предполагают финансовых или временных затрат. Естественно, что подобные способы не гарантируют стопроцентного избавления от вредных веществ.
Наиболее распространенным методом считается кипячение. Снизить концентрацию солей способна термическая обработка. Этот способ вызывает массу нареканий у специалистов. Во-первых, при кипячении избыток веществ оседает на стенках посуды, в которую помещен раствор. Накипь очень трудно отмыть. Во-вторых, после кипячения из напитка вымываются не только вредные компоненты, но и полезные. Человеку нельзя употреблять только термически обработанную воду, поскольку недостаток микроэлементов пагубно скажется на здоровье.
Еще один доступный способ – отстаивание. Соли осядут на дне емкости, но их концентрация снизится незначительно. Поэтому такой метод считается не самым эффективным.
Если требуется смягчить раствор, предназначенный для стиральной машины, используйте специальные магазинные средства. Они выпускаются в виде таблеток и используются при каждой стирке, защищая нагревательные приборы бытовой техники от образования накипи.
Единицы измерения
Мы объяснили, какую воду называют жесткой, чем обусловлена общая жесткость и какие виды различают, теперь обсудим, в чем измеряется показатель и что на него влияет.
К сожалению, нет мирового стандарта, поэтому, используя аппаратуру европейского изготовления, будьте готовы к непонятным на первый взгляд обозначениям. Российскими учеными были установлены следующие единицы – моль на кубический метр. А перед этим ставится число, которое соответствует значению перевоплощения в миллиграммы на литр. А что можно встретить еще:
- d° или dH – придумали в Германии, но применяют на всей территории Запада;
- f° – пишут во Франции;
- ppm CaCO3 – используют в США.
Что влияет на норму?
Выделяют следующие факторы, влияющие на содержание магния, кальция, карбонатов, меняющих состав:
- Природа воды (водопроводная, дистиллированная, талая, родниковая, кипяченая).
- Состав водопроводной воды в определенной местности.
- Виды обитателей и продукты их метаболизма (рыбки, черепахи, водоросли).
- Период, за который не меняют воду, не очищают аквариум.
- Наличие или отсутствие фильтрации воды.
- Декор (гравий, крупные камни, замки).
- Наличие или отсутствие прямых солнечных лучей, падающих на растительность.
Даже если водопроводная вода в определенной местности обладает чрезмерными карбонатными показателями, их можно урегулировать
Это важно для аквариумов, где разводят дорогостоящие виды рыб
Как избавиться от жесткости воды и от чего она зависит

Если перед вами стоит вопрос что делать непосредственно с водопроводной жесткой водой, то выходов из ситуации не много:
- поставить фильтр внутри квартиры, регулярно проверять систему и менять кассеты;
- кипячение – стоит учесть, что данным способом можно убрать только карбонатный осадок, он останется внизу чайника или на его стенках, но если примесь в виде магниевых и кальциевых солей, способ не подходит;
- заморозка – емкость следует проморозить так, чтобы на 90% образовался лед, а остальные 10% – слить, ведь именно концентрированный раствор замораживается медленнее всего.
Как повысить и понизить жесткость в аквариуме

Аквариумные рыбки – очень прихотливые создания, даже морские виды. У них всегда есть пределы, родной ареал обитания. Если вы хотите, чтобы они жили и размножались, следует воссоздать все необходимые условия.
Если нужно увеличить показатель солей, на дно можно положить известняк или мрамор, добавить хлористый кальций или магнезию.
В обратном случае придется прибегнуть к одному из вышеперечисленных трех способов. Чем больше объем резервуара, тем выгоднее будет создание фильтрационной системы.
Как избавиться от примесей в скважине
При бурении индивидуальной точки доступа к ресурсу просто необходимо делать предварительный анализ. Очень часто от этого зависит выбор расположения, а также глубина пролегания труб и насоса. Но если на участке испорченные грунтовые воды, поскольку они протекают через многочисленные солесодержащие почвенные слои, то и выбор места особенно не поможет, нужно производить фильтрацию. Обратитесь в , чтобы специалисты выбрали для вас индивидуальное комплексное решение.
Диспенсер магистральный настольный AquaPro 919H/RO (горячая и холодная вода)
Диспенсер магистральный настольный AquaPro 929CH/RO (охлаждение/нагрев)
Диспенсер напольный AquaPro 311 (пустой, без охлаждения)
Параметры, какая должна быть
Разные виды рыб выживают и размножаются в определенных условиях. Для одних оптимальна низкая жесткость, для других – средняя.
Но выделяют наиболее оптимальные параметры:
- 3-6 мг-экв/л карбонатной жесткости для недавно налитой воды.
- до 15 мг-экв/л, когда вода стоит долго.
На жизнедеятельность внутренней среды аквариума негативно влияет чрезмерно пониженная или повышенная жесткость. Это критические параметры.
| Вид критического параметра | Описание |
| Низкий | Происходит по причине недостатка или отсутствия кальция. Без него растительность существовать не может, так как прекращается ее рост. Поэтому минимальное значение составляет 4 мг-экв/л |
| Высокий | Приводит к выпадению осадка, постепенной гибели рыб. В такой среде затруднено дыхание, размножение, другие основные функции. Критичность появляется свыше 15 мг-экв/л |
Оптимальными считаются мягкие или средние показатели. Они колеблются при изменении внешних и внутренних факторов. Поэтому периодически делают замер тест-системой.
Способы умягчения воды
- Самый простой и чудесный метод – элементарное кипячение воды, о котором было написано выше.
- Простейший химический способ – добавить гашенной извести.
Если два первых метода относились к карбонатной жесткости, то с постоянной жесткостью бороться сложнее. Но и это вполне реально:
- Вымораживание льда. Нужно не до конца заморозить воду и слить оставшиеся примерно 10%. Лед разморозить, он будет свободен от солей.
- Перегонка с испарением воды, так как соли не являются летучими веществами.
Теперь промышленные технологии избавления:
- Действие магнитных полей.
- Промышленная катионная очистка с реагентами и последующим определением карбонатной жесткости.
- Самый эффективный способ – осмос с фильтрами для обмена ионами, в результате чего «жесткие» соли заменяются на «мягкие».
В чем измеряется жесткость воды?
Для количественного измерения любых наблюдаемых природных процессов придуманы особые единицы, не исключение и жесткость воды. Так как способов ее лабораторного определения несколько, соответственно, в науке закрепились различные единицы измерения.

В России с 2014 года для измерения жесткости воды принята особая единица – градус жесткости (°Ж), именно она внесена в ГОСТ. Градус жесткости связан с единицей измерения, принятой для измерения количества вещества в химии, – моль. В 1°Ж содержится 0,5 миллимоль ионов металла на литр. А также для измерения жесткости воды применяют особую единицу миллиграмм-эквивалент на литр (мг-экв/л). Российский градус жесткости равняется 1 мг-экв/л. Градусы жесткости в разных странах чаще всего не совпадают, по этой причине, чтобы перевести градус жесткости, принятый в какой-либо стране, в российские градусы жесткости приходится использовать специальные рассчитанные профессионалами таблицы.
Например, американский градус жесткости примерно равняется 0,02°Ж, немецкий – 0,35°Ж, английский – 0,28°Ж, французский – 0,19°Ж. Учет разницы единиц измерения может быть актуален в случае приобретения импортной бытовой техники или моющих средств непосредственно в стране-изготовителе.
Химически жесткость обусловлена присутствием в воде ионов металлов и некоторых анионов, возникающих при диссоциации растворимых солей. Поступают такие вещества в воду из горных пород. Именно минеральный состав грунта определяет наличие солей в растворах. Концентрация солей может изменяться сезонно. Наибольшая концентрация отмечается для начала весны, так как в это время на фоне полного отсутствия притока чистой воды из атмосферных осадков: талой от снега и дождевой, практически лишенных растворенных солей, уровень воды в грунте существенно уменьшается.

При этом некоторые ионы из раствора удаляются кипячением, в результате жесткость может быть снижена. Это так называемая временная или карбонатная жесткость. Повышение температуры вызывает ускоренную реакцию гидрокарбонатного аниона (HCO 3-) с находящимися в воде катионами Ca 2+, в результате которой образуется малорастворимый осадок карбоната кальция СаСО3, покрывающий поверхность посуды или нагревательный элемент тем, что принято называть «накипь». Вместе с паром в воздух уходит некоторое количество образовавшегося в ходе реакции углекислого газа СО2, также в результате реакции образуются молекулы воды (Н2О).

Постоянная жесткость воды обусловлена прежде всего наличием в растворе ионов Са2+ и Mg2+, а также некоторых других катионов. Главными их источниками являются растворимые осадочные горные породы, через слои которых проходит вода: известняки, доломиты, гипс и некоторые другие. Ионы железа могут поступать и при взаимодействии воды со стенками трубопроводов – особенно это заметно, если сроки эксплуатации систем накопления и распределения воды значительно превышены. Связать в нерастворимые соли эти ионы кипячением не получится, а если в воде мало или отсутствуют гидрокарбонатные анионы, не свяжется и кальций.

Общая жесткость складывается из показателей постоянной и временной жесткости, так как для некипяченой «сырой» воды, характерной для природного источника (например, скважины), или поступающей из водопровода определяться лабораторно будет именно она. Эта жесткость и измеряется по ГОСТу в°Ж.
В России мягкой считается вода, имеющая не более 2°Ж, высокую жесткость имеет раствор с 10°Ж и более. От 2°Ж, до 10°Ж имеет жидкость со средним показателем этого параметра.

Как измерить и понять, допустимая или повышенная жесткость – способы

Представляем три варианта:
- Наиболее точный – заказать лабораторный анализ. Во время пристального изучения будет произведен разбор на химические вещества, поэтому справка не только покажет общий показатель, но и конкретное содержание микроэлементов – какие и в каком объеме присутствуют в образце. Необходимо делать такую экспертизу владельцам частных домов при оборудовании скважины или колодца и заказе фильтрационной системы.
- Быстрый и доступный каждому. Для этого стоит приобрести тестер в виде бумажной полоски. Его нужно опустить в жидкость, подождать указанный период, а затем определить цвет индикатора. Дело в том, что на активную части нанесен реагент, который вступает в реакцию и показывает количество примесей. Минус в сложности интерпретации и достаточно неточных результатах.

Домашний химический опыт. В два одинаковых мерных стакана следует нарезать по одному грамму хозяйственного мыла 72%. Затем залейте их подогретой водой – в одну емкость дистиллированной, во вторую водопроводной. В первом бокале будет уровень 7 см. А во втором – остановитесь вливать жидкость в тот момент, когда появится мыльная пена. Затем измерьте разницу влитой влаги. Каждый 1 см раствора соответствует двум °dH.
Как смягчить воду
Итак, способов узнать, насколько жесткая вода, довольно много. Если вы обнаружили, что качество воды вас не устраивает, то воспользуйтесь некоторыми советами.
1. Самый известный метод, которым пользуются все, не задумываясь об истинном предназначении, это кипячение воды. Достаточно прокипятить воду в течение часа, а затем дать ей остыть, как на дне образуется осадок. В дальнейшем убрать его можно путем процеживания. Конечно, таким способом избавиться от солей не удастся, а вот немного смягчить воду представится возможным.
2. Нейтрализовать соль можно щелочью, которая содержится в соде. ¼ чайной ложки на стакан воды – и степень жесткости заметно уменьшена. Многие проверили это на практике!
Предлагаем ознакомиться Как отбелить вещи «Белизной»: полезные советы
3. Щелочь можно заменить миндальными отрубями. Они являются конечным продуктом переработки семян миндаля. Столовой ложки на стакан воды вполне хватит.
4. Наиболее простым вариантом является покупка специального фильтра. Однако исследование мнений пользователей на основе отзывов показало, что эффективности в использовании фильтров не наблюдается. Более того, необходимо постоянно следить за системой очистки воды и периодически менять некоторые элементы. Зачастую своевременно это сделать не представляется возможным, и вредные вещества снова оказываются в воде.
Использование мягкой и жесткой воды
Однозначного ответа на вопрос, какая же вода лучше – мягкая либо жесткая, нет. Каждая из них имеет свои положительные и отрицательные стороны. Однако жесткая вода из-под крана, содержащая большое количество солей, конечно, вредна для нашего здоровья.
С другой стороны, чересчур мягкая вода также имеет свои минусы – она вымывает из крови необходимые организму микроэлементы, что существенно увеличивает вероятность развития сердечно-сосудистых заболеваний.
На самом деле организму могут наносить больший вред другие вещества, входящие в состав жидкостей. К минусам жесткой воды можно отнести возникновение известняковых отложений на стенках бытовых приборов. Также практически все моющие средства очень плохо пенятся, зато жир с поверхности кожи смывается очень хорошо. А это, в свою очередь, грозит раздражением.
Отрицательным качеством является также и то, что волосы после мытья становятся непослушными и жесткими. Появляется риск образования в почках и печени камней, а в суставах – солей. Среди положительных качеств жесткой воды можно выделить разве что вероятность снижения развития гипертонических болезней и заболеваний сердца.
Зачем надо знать TDS и где это применяется?

Первое и, наверное, самое важное — это химическая чистота исходной воды. Почти все профессиональные акваскейперы используют фильтры обратного осмоса для создания своих аквариумов
Это специальные фильтры, устанавливающиеся в магистрали водопровода вашего дома или квартиры, наподобие обычных бытовых фильтров, с той лишь разницей, что пить такую воду нельзя и она используется в специализированных целях, одна из которых, как раз, аквариум с растениями.
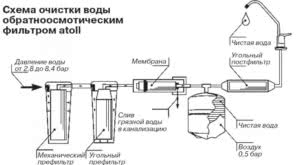 Степень очистки воды контролируется как раз параметром TDS.
Степень очистки воды контролируется как раз параметром TDS.
Обратноосмотический фильтр состоит из префильтров: фильтра механической очистки и угольного фильтра, а также мембраны — основного элемента обратноосмотического фильтра.
Префильтры служат в качестве защиты мембраны для увеличения её срока работы.
При TDS из водопровода ~ 300 картридж угольного фильтра расходуется в течение недели, картридж механической очистки — в течение двух недель, а вот состояние мембраны можно оценить только по TDS.
Обычно, после мембраны устанавливаются фильтры с деионизирующей смолой. Он “добивает” остаточный TDS после мембраны с 3-4 до 0 ppm.


Я рекомендую использовать именно такую воду (0 ppm) в растительных аквариумах, т. к. оставляя TDS после осмоса на значении отличном от нуля, мы не знаем, что же остаётся в этой воде, т. к. мы видели ранее, что TDS состоит из большого количества различных составляющих.
 Состояние ионообменных смол также контролируется с помощью TDS. Таким образом, при использовании воды после обратного осмоса TDS мы контролируем дважды.
Состояние ионообменных смол также контролируется с помощью TDS. Таким образом, при использовании воды после обратного осмоса TDS мы контролируем дважды.
После мембранного фильтра и после ионообменных смол.
Компания SpectraPure предусмотрела необходимость часто измерять TDS, поэтому встроила в свои фильтры электронные TDS-метры. В некоторых фильтрах этой фирмы их даже два.
Способы определения уровня жесткости
 Жильцам многоквартирных и частных домов желательно знать уровень жесткости воды. Делается это в таких целях:
Жильцам многоквартирных и частных домов желательно знать уровень жесткости воды. Делается это в таких целях:
- установить правильные программы на бытовую технику;
- купить оптимальный картридж для умягчения воды;
- подобрать правильные дозировки смягчающих средств;
- обеспечить оптимальные условия для аквариумных обитателей;
- подобрать надежную и эффективную фильтровальную систему.
Самостоятельно определить уровень минерализации жидкости можно несколькими способами.
Точный анализ
Забранный образец относят в местную СЭС. Для жидкости нужно подобрать чистую полимерную тару. Объем материала для исследования — 1-2 литра. В санэпидемстанции не только определят концентрацию растворенных солей в воде, но и выявят наличие пестицидов, нитратов, сероводорода, марганца, железа, органики. Особенно хорош анализ для подбора правильной фильтровальной установки или системы смягчения воды.
Применение тест-полосок
Это быстрый способ определения качества жидкости. Купить индикаторы можно в зоологических магазинах или точках продаж чая-кофе. Специальный реагент, нанесенный на тестовую полоску, окрашивается в определенный цвет при контакте с растворенными минералами. Интенсивность колера говорит об уровне концентрации солей в воде, то есть о степени её жесткости. Чем ярче цвет, тем больше растворенных солей в имеющемся образце.
Проведение домашнего опыта
Потребуются теплая дистиллированная вода и кусок хозяйственного мыла 72%. Из оборудования под рукой нужно иметь стакан, прозрачную литровую ёмкость (можно банку), электронные весы и линейку.
Действуют при проведении опыта таким образом:
- На мелкую терку натирают мыло и отмеряют 1 грамм. Готовую массу опускают в пустой стакан.
- Дистиллированную воду греют до 60-70 градусов и выливают туда же. Мыло должно полностью раствориться.
- В стакан доливают еще дистиллированной жидкости из расчета для мыла 72% — 7 см, для мыла 60% — 6 см.
- В банку загружают 0,5 л водопроводной (скважинной, колодезной) жидкости.
- Сюда же медленно переливают дистиллированный мыльный раствор и помешивают все до образования пены, которая говорит о том, что хозяйственное мыло связало все минеральные соли.
- Остаётся измерить высоту жидкости ниже пены и вычесть её из исходного уровня в банке. Это и будет примерная концентрация растворенных минералов в воде.
Подобный опыт хоть и интересен, повышенной точностью не отличается.
Жесткость воды. Соли жесткости
Жесткость воды — это совокупность химических и физических свойств воды, связанных с содержанием в ней растворенных солей щелочноземельных металлов, главным образом, кальция и магния (так называемых «солей жесткости»).
Соли жесткости имеют разные свойства. Так, при нагреве воды, некоторые из них выпадают в осадок в виде накипи, а некоторые — не выпадают. По этому признаку их и начали разделять.
Соли, выпадающие в осадок, стали называть солями временной (или устранимой) жесткости, а соли, которые не выпадают в осадок при нагреве воды, солями постоянной жесткости.
Сульфаты, хлориды и нитраты магния и кальция, растворенные в воде, образуют постоянную (или некарбонатную) жесткость. Они выпадают в осадок исключительно при полном испарении воды.
Временная жесткость характеризуется присутствием в воде наряду с катионами Ca2+, Mg2+ и Fe2+ гидрокарбонатных, или бикарбонатных анионов (HCO3-).
При кипячении воды гидрокарбонаты разлагаются, образуя очень плохо растворимый карбонат кальция, углекислый газ и воду:
Общая жесткость складывается из постоянной и временной.
В данной таблице приведены основные катионы металлов, вызывающие жесткость, и главные анионы, с которыми они ассоциируются.
| Катионы | Анионы |
| Кальций (Ca2+) | Гидрокарбонат (HCO3-) |
| Магний (Mg2+) | Сульфат (SO42-) |
| Стронций (Sr2+) | Хлорид (Cl-) |
| Железо (Fe2+) | Нитрат (NO3-) |
| Марганец (Mn2+) | Силикат (SiO32-) |
На практике стронций, железо и марганец оказывают на жесткость столь небольшое влияние, что ими, как правило, пренебрегают. Алюминий (Al3+) и трехвалентное железо (Fe3+) также влияют на жесткость, но при уровнях рН, встречающихся в природных водах, их растворимость и, соответственно, «вклад» в жесткость ничтожно малы. Аналогично, не учитывается и незначительное влияние бария (Ва2+).
Жёсткость воды — происхождение
Ионы кальция (Ca2+) и магния (Mg2+), а также других щелочноземельных металлов, обуславливающих жесткость, присутствуют во всех минерализованных водах. Их источником являются природные залежи известняков, гипса и доломитов.
Ионы кальция и магния поступают в воду в результате взаимодействия растворенного диоксида углерода с минералами и при других процессах растворения и химического выветривания горных пород.
Источником этих ионов могут служить также микробиологические процессы, протекающие в почвах на площади водосбора, в донных отложениях, а также сточные воды различных предприятий.
Обычно в маломинерализованных водах преобладает (до 70%-80%) жесткость, обусловленная ионами кальция (хотя в отдельных редких случаях магниевая жесткость может достигать 50-60%).
С увеличением степени минерализации воды содержание ионов кальция (Са2+) быстро падает и редко превышает 1 г/л.
В целом, жесткость поверхностных вод, как правило, меньше жесткости вод подземных. Жесткость поверхностных вод подвержена заметным сезонным колебаниям, достигая обычно наибольшего значения в конце зимы и наименьшего в период половодья, когда обильно разбавляется мягкой дождевой и талой водой. Морская и океанская вода имеют очень высокую жесткость (десятки и сотни мг-экв/дм3).
Жесткость воды — единицы измерения
С 1 января 2014 года в России введен межгосударственный стандарт ГОСТ 31865-2012 «Вода. Единица жесткости». По новому ГОСТу жесткость выражается в градусах жесткости (°Ж).
1 °Ж соответствует концентрации щелочноземельного элемента, численно равной 1/2 его миллимоля на литр (1 °Ж = 1 мг-экв/л). В разных странах использовались (иногда используются до сих пор) различные внесистемные единицы — градусы жёсткости.
За рубежом приняты другие единицы измерения жесткости воды, соотношение этих единиц представлено ниже:
1°Ж = 20,04 мг Ca2+ или 12,15 Mg2+ в 1 дм3 воды;
1°DH = 10 мг CaO в 1 дм3 воды;
1°Clark = 10 мг CaCO3 в 0,7 дм3 воды;
1°F = 10 мг CaCO3 в 1 дм3 воды;
1 ppm = 1 мг CaCO3 в 1 дм3 воды.
Численные значения жесткости измеренные в мг-экв/л, моль/м3, и °Ж, несмотря на различия в обозначении, равны между собой.
По значению общей жесткости природные воды делят на группы:
- очень мягкая вода (0–1,5 мг-экв/л)
- мягкая вода (1,5–4 мг-экв/л)
- вода средней жесткости (4–8 мг-экв/л)
- жесткая вода (8–12 мг-экв/л)
- очень жесткая вода (более 12 мг-экв/л).
Нормативные требования и рекомендации
Рекомендации всемирной организации здравоохранения (ВОЗ) для питьевой воды:
кальций – 20-80 мг/л; магний – 10-30 мг/л. Для жесткости какой-либо рекомендуемой величины не предлагается.
Как повысить и понизить жесткость воды в аквариуме. Определение временной, или карбонатной жесткости
Чтобы создать комфортные условия для жизни аквариумных рыбок, важно использовать воду оптимальной жесткости, с заданным кислотно-щелочным балансом. Чтобы повысить жесткость воды, используют известняк и мрамор
Чем мягче вода, тем быстрее она повысит жесткость. Другой способ – химический, с применением хлористого кальция и магнезии
Чтобы повысить жесткость воды, используют известняк и мрамор. Чем мягче вода, тем быстрее она повысит жесткость. Другой способ – химический, с применением хлористого кальция и магнезии.
Максимальный эффект достигается при использовании обоих препаратов одновременно.
Чтобы уменьшить жесткость, воду нужно прокипятить. Как долго это следует делать? Учтите, что для снижения жесткости вдвое, кипятить воду нужно минимум в течение получаса. Другой способ – вымораживание. Воду наливают в пластиковый контейнер и помещают в морозилку. Затем лед растапливают, а полученную воду используются в пищевых или любых других целях.
Если объемы воды большие, проще будет использовать специальное оборудование. Широкое распространение в быту в последние годы получили установки обратного осмоса. Для расчета необходимого объема водопроводной воды используйте формулу – вычитание объема воды, получаемой из водопровода, из объема с заданной жесткостью, который нужно получить.
Часто методы умягчения используют комбинированно. Например, одну часть солей жесткости убирают реагентным способом, а другую с помощью катионного обмена. Приведем формулы содово-известкового способа умягчения:
Са(НСО3)2 + Са(ОН)2 = 2СаСО3 + 2Н2О
В итоге Mg(OH)2 коагулирует, выпадая в осадок. Затем, в целях устранения некарбонатной жесткости, вводится Na2CO3.
Последующие химические реакции:
В итоге образуется углекислый кальций, выпадающий затем в осадок. Реагенты вводят в разные зоны:
- хлор – во всасывающие трубопроводы;
- коагулянт – в трубопровод перед смесителем либо непосредственно в смеситель;
- известь – вместе с коагулянтом;
- уголь активированный – перед фильтрами;
- хлор и аммиак – в фильтрованную воду.
Опреснение, обессоливание, удаление растворенных газов, железа, стабилизация – это специальные способы очистки. Так если для снижения жесткости используются методы катионирования или ионного обмена, речь идет об обессоливании. Вода, которая получается на выходе, не содержит ни анионов, ни катионов солей.
Как измерить жесткость
Для оценки показателей жесткости воды используются следующие способы:
- Комплексонометрическое титрование трилоном Б. Метод сложный и самый точный.
- Покупные тесты. Не на 100% точные, зато простые и недорогие.
- Измерение электропроводности. Используйте кондуктометр.
- С помощью ионометра и ионоселективных электродов.
- С применением методики титрования соляной кислотой проб воды. Сложный и не очень точный метод. То же самое можно сказать о тестах с применение хозяйственного мыла.
Под титрованием подразумевается добавление в воду реагента требуемой концентрации. Концентрация солей жесткости определяется в зависимости от реакции реагента с водой. Приготовить реактив просто – достаточно смешать кислоту с дистиллированной водой в заданных пропорциях. Готовый раствор опасности не представляет.
Проще всего использовать готовые тексты. Для этого 5 мл воды наливается в стаканчик, затем в жидкость по каплям добавляется содержимое теста, после каждой капли вода перемешивается. Делать так нужно до тех пор, пока цвет не станет зеленым вместо розового.